Terapeutické peptidy

Terapeutické peptidy sú jedinečnou triedou farmaceutických činidiel zložených zo série dobre usporiadaných aminokyselín, zvyčajne s molekulovou hmotnosťou 500 — 5 000 Da. Výskum terapeutických peptidov sa začal základnými štúdiami prirodzených ľudských hormónov vrátane inzulínu, oxytocínu, vazopresínu a hormónu uvoľňujúceho gonadotropín (GnRH) a ich špecifických fyziologických aktivít v ľudskom tele. Od syntézy prvého terapeutického peptidu – inzulínu – v roku 1921 sa dosiahli pozoruhodné úspechy, ktorých výsledkom bolo schválenie viac ako 80 peptidových liečiv na celom svete. Vývoj peptidových liečiv sa tak stal jednou z najhorúcejších tém farmaceutického výskumu.
Prvá polovica 20. storočia bola svedkom objavu niekoľkých život zachraňujúcich bioaktívnych peptidov, ako je inzulín či adrenokortikotropný hormón, ktoré boli pôvodne študované a izolované z prírodných zdrojov. Objav a vývoj inzulínu – peptidu s 51 aminokyselinami – bol považovaný za jeden z monumentálnych vedeckých úspechov v objavovaní liekov. Prvýkrát ho izoloval Frederick Banting v roku 1921 a ďalej ho vyvinuli Frederick a Charles Best a už rok po jeho prvej izolácii bol dostupný pre pacientov s diabetes mellitus. V roku 1923 sa inzulín stal prvým komerčným peptidovým liekom a odvtedy je prospešný pre tisícky pacientov s cukrovkou. Produkcia ľudského inzulínu počas 20. storočia však nedokázala držať krok kvôli vysokému dopytu a na trh sa dostali inzulíny živočíšneho pôvodu, ako napríklad hovädzí a bravčový inzulín, ktoré dominovali na trhu s ľudským inzulínom takmer 90 rokov, kým ich nenahradil rekombinantný inzulín.
Vývoj peptidových liekov vstúpil do novej éry s príchodom 21. storočia, odkedy pokroky v štrukturálnej biológii, rekombinantnej biológii a nových syntetických a analytických technológiách tento proces výrazne urýchlili. Bol vytvorený sofistikovaný systém vývoja peptidových liekov, vrátane objavovania peptidových liekov, dizajnu liekov, syntézy peptidov, štruktúrnej modifikácie a hodnotenia aktivity. Od roku 2000 bolo na celom svete schválených celkovo 33 neinzulínových peptidových liečiv. Okrem toho tieto peptidové lieky už nie sú len napodobňovaním hormónov alebo jednoducho zložené z prírodných aminokyselín. Napríklad enfuvirtid je 36-aminokyselinový biomimetický peptid napodobňujúci proteíny vírusu ľudskej imunodeficiencie (HIV) používané v kombinovanej terapii na liečbu; zikonotid je neurotoxický peptid odvodený zo slimáka Conus magus, schválený bol v roku 2004 a používa sa na zvládanie ťažkej chronickej bolesti; teduglutid je analóg glukagónu podobného peptidu 2 (GLP-2) používaný na liečbu syndrómu krátkeho čreva a vyrába sa pomocou kmeňa Escherichia coli modifikovaného technológiou rekombinantnej DNA; liraglutid je peptid skladajúci sa z 31 aminokyselín a jeho štruktúra je odvodená z ľudského GLP-1 (7 – 37), vzniká substitúciou lyzínu v pozícii 34 s arginínom a pripojením palmitoylovanej glutámovej kyseliny na lyzín v pozícii 26, pôsobí ako agonista GLP-1 receptora pri zvládaní diabetes mellitus 2. typu (T2DM).
Všetky peptidové liečivá sa používajú v širokom rozsahu terapeutických oblastí, ako je urológia, pneumológia, liečba bolesti, onkológia, metabolické, kardiovaskulárne a antimikrobiálne ochorenia. K dnešnému dňu je viac ako 170 peptidov v aktívnom klinickom vývoji, s mnohými ďalšími v predklinických štúdiách.
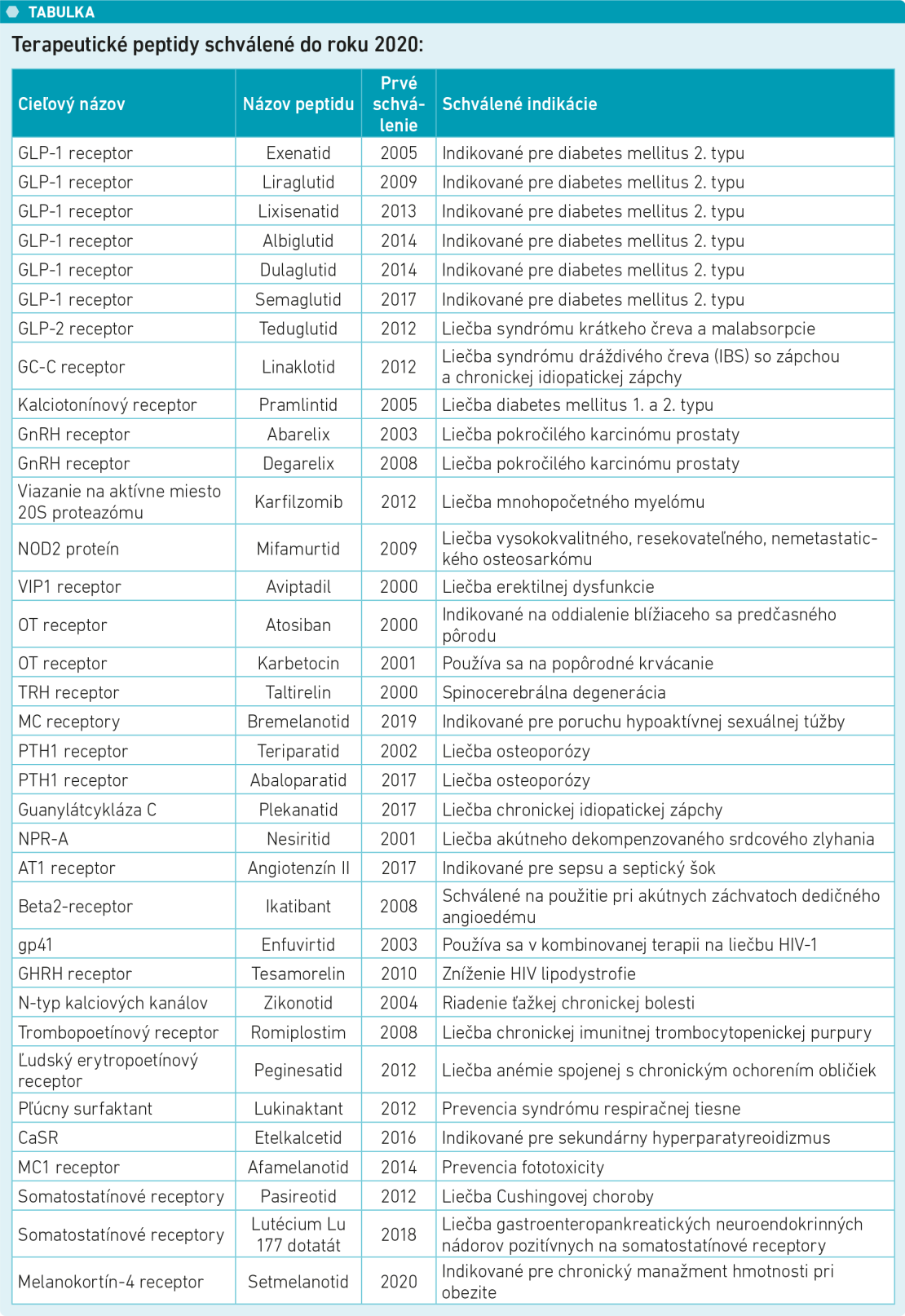
Terapeutické peptidy schválené do roku 2020:
Farmakodynamické interakcie, aditívne/synergické účinky:
Kombinácia peptidov s inými liekmi, ktoré majú podobné terapeutické účinky, môže viesť k aditívnym alebo synergickým účinkom. Napríklad kombinácia agonistov GLP-1 receptora (ako je exenatid) s inými antidiabetikami (napr. inzulínom, metformínom) môže zosilniť účinky na zníženie koncentrácie glukózy, čo môže viesť k hypoglykémii.
Antagonistické účinky: Naopak, niektoré lieky môžu pôsobiť proti účinkom terapeutických peptidov. Napríklad kortikosteroidy by mohli znížiť účinnosť peptidov kvôli ich protichodným účinkom na hladinu glukózy v krvi.
Špecifické liekové interakcie s agonistami receptora pre glukagónu podobný peptid-1 (GLP-1 (napr. exenatid, liraglutid): Môžu interagovať s liekmi, ktoré spomaľujú vyprázdňovanie žalúdka, ako sú opioidy, čo môže zvýšiť účinky GLP-1 agonistov na spomalenie motility žalúdka. Táto interakcia môže ovplyvniť absorpciu súbežne užívaných perorálnych liekov.
Analógy somatostatínu (napr. pasireotid): Môžu inhibovať sekréciu rôznych hormónov a môžu interagovať s liekmi, ktoré závisia od týchto hormónov, ako je inzulín, perorálne hypoglykemické lieky alebo lieky, ktoré ovplyvňujú os hypofýza-nadobličky.
Angiotenzín II (používaný pri septickom šoku): Pri použití s inými vazopresormi alebo liekmi, ktoré ovplyvňujú krvný tlak, je potrebné starostlivé sledovanie, aby sa predišlo nadmerným zmenám krvného tlaku.
Zikonotid (blokátor vápnikového kanála typu N): Keď sa používa na silnú bolesť, môže interagovať s inými látkami tlmiacimi centrálny nervový systém, čím sa zvyšuje riziko sedácie alebo útlmu dýchania.
Vplyv chorobných stavov, poškodenie funkcie obličiek alebo pečene: U pacientov s poškodením funkcie obličiek alebo pečene môže byť metabolizmus a vylučovanie peptidov a súčasne podávaných liekov zmenené, čo vedie k zvýšenému riziku toxicity alebo k zníženiu účinnosti.
Monitorovanie a riadenie, terapeutické monitorovanie liekov: Pravidelné monitorovanie hladín liekov a reakcií pacienta je nevyhnutné, keď sa peptidy používajú s inými liekmi, najmä v prípadoch, keď sú pravdepodobné interakcie.
Úprava dávkovania: Na udržanie terapeutickej účinnosti pri minimalizácii nežiaducich účinkov môže byť potrebná úprava dávky buď peptidu, alebo interagujúceho liečiva.
Zdroje:
- Craik DJ. The future of peptide-based drugs. Chem Biol Drug Des 2013;81:136–147.
- Lau JL, Dunn MK. Therapeutic peptides: historical perspectives, current development trends, and future directions. Bioorg Med Chem 2018;26:2700–2707.
- Drucker DJ. The discovery of GLP-2 and development of teduglutide for short bowel syndrome. ACS Pharmacol Transl Sci 2019;2:134–142.
- doi: 10.1021/acsptsci.9b00016. eCollection 2019 Apr 12.
- Beltran JV. Peptide Therapy: Healing, Benefits & Side Effects | Healthnews, November 16, 2023.
- Frontiers | Therapeutic Peptides Targeting PPI in Clinical Development: Overview, Mechanism of Action and Perspectives (frontiersin.org).
- Table by Martina Pardusova.